- Бета-амилоид – компонент врожденного иммунитета?
- Выведение бета-амилоида болезни Альцгеймера из головного мозга уменьшается с возрастом
- Более низкие значения выведения бета-амилоида 42 у людей с симптомами болезни Альцгеймера
- К кому обратится:
- Амилоидные бляшки при болезни Альцгеймера – «уборка» биологического мусора?
- Клинические рекомендации по диагностике и лечению системного амилоидоза
- Определение, классификация, группы риска и принципы диагностики
- Рекомендации:
- Клинические проявления
- Рекомендации:
- Лечение системного амилоидоза
- Лечение АА-амилоидоза
- Рекомендации:
- Лечение АL-амилоидоза
- Рекомендации:
- Лечение ATTR-амилоидоза
Бета-амилоид – компонент врожденного иммунитета?
В статье «The Alzheimer’s Disease-Associated Amyloid β-Protein Is an Antimicrobial Peptide», опубликованной в журнале PLoS One от 3 марта, исследователи, работающие под руководством Роберта Моира (Robert D. Moir) из Центральной больницы штата Массачусетс, описывают полученные ими доказательства антимикробных свойств бета-амилоида. Судя по всему, этот белок является компонентом врожденного иммунитета, обеспечивающим защиту организма от широкого спектра патогенов.
Врожденный иммунитет является первой линией защиты организма от проникающих в него патогенов. Запуск механизмов врожденного иммунного ответа обеспечивает быструю мобилизацию лейкоцитов и химических факторов, таких как цитокины и антимикробные пептиды, на борьбу с бактериями, вирусами, грибками и даже опухолевыми клетками. Антитела и другие компоненты приобретенного иммунного ответа практически не проникают в окруженные гематоэнцефалическим барьером ткани головного мозга, поэтому защита центральной нервной системы от инфекций преимущественно является задачей антимикробных пептидов.
Бета-амилоид токсичен для нейронов и его накопление, приводящее к появлению характерных бляшек в тканях мозга пациентов с болезнью Альцгеймера, считается причиной развивающихся при этом заболевании симптомов нейродегенерации. Этот протеин является продуктом ферментативного расщепления более крупных молекул белка-предшественника, при котором образуется несколько типов молекул бета-амилоида. Наиболее распространенные из них – бета-амилоид-40 и бета-амилоид-42 – особенно склонны к формированию токсичных бляшек. Известно, что бета-амилоид стимулирует воспалительные процессы, а его биологическая активность до сих пор считалась исключительно патогенной. Однако авторы получили доказательства того, что на самом деле бета-амилоид обладает антимикробными свойствами и может играть важную роль в защите головного мозга от инфекций.
Сначала ученые заметили, что бета-амилоид обладает определенным физическим, химическим и биологическим сходством с антимикробными белками, в особенности человеческим кателицидином LL-37. С целью изучения этого феномена они провели параллельное тестирование микробицидной активности бета-амилоидов-40 и -42 и LL-37 с помощью панели из 15 наиболее важных патогенов. В результате оказалось, что бета-амилоид подавляет рост восьми из них. При этом, по сравнению с LL-37, бета-амилоид-40 был более эффективен против семи, а бета-амилоид-42 – против шести из этих микроорганизмов, в том числе против дрожжеподобного грибка Candida albicans и определенных штаммов листерий, стрептококков и стафилококков.
Для изучения антимикробной активности бета-амилоида, ассоциированного с болезнью Альцгеймера, исследователи протестировали способность посмертных образцов гомогенизированной ткани мозга пациентов с болезнью Альцгеймера и контрольных индивидуумов такого же возраста подавлять рост дрожжеподобного грибка Candida albicans в культуре. Наибольшая концентрация бета-амилоидных бляшек, как правило, наблюдается в лобных долях головного мозга, и образцы этих участков мозга пациентов с болезнью Альцгеймера в значительной степени подавляли рост грибков, чего не наблюдалось в культурах, в которые вносили контрольные образцы ткани. При этом степень микробицидности образцов была прямо пропорциональна количеству содержащегося в них бета-амилоида, а внесение в культуру антител к бета-амилоиду возобновляло рост возбудителей. Результаты второго эксперимента, при проведении которого использовались образцы ткани мозжечка, для которого характерно наиболее низкое содержание бета-амилоида, как в экспериментальной, так и в контрольной постановках продемонстрировали отсутствие антимикробной активности.
Авторы предполагают, что продолжительная активация механизмов врожденного иммунитета в результате хронической или перенесенной инфекции центральной нервной системы может приводить к избыточной продукции и накоплению бета-амилоида. Известные факторы риска развития болезни Альцгеймера, такие как инсульт, черепно-мозговые травмы и воздействие определенных анестетиков, также могут запускать механизмы врожденного иммунного ответа и стимулировать продукцию бета-амилоида.
Тогда как редкая мутация, непосредственно вызывающая развитие наследственной формы болезни Альцгеймера, стимулирует синтез бета-амилоида-42, несколько недавно идентифицированных генов, предположительно играющих роль в патогенезе заболевания, участвуют в формировании врожденного иммунитета. В настоящее время исследователи проверяют гипотезу, согласно которой комплекс генетических факторов может повышать вероятность развития болезни Альцгеймера посредством активации механизмов врожденного иммунитета и, соответственно, стимуляции синтеза бета-амилоида.
Авторы считают, что идентификация патогенов, наиболее склонных к запуску синтеза бета-амилоида, позволит разработать методы профилактики и подавления этого механизма, например, посредством иммунизации.
Источник
Выведение бета-амилоида болезни Альцгеймера из головного мозга уменьшается с возрастом
После 65 лет риск развития болезни Альцгеймера удваивается каждые 5 лет. Теперь новое исследование обнаружило, что способность головного мозга выводить токсические фрагменты белка, связанные с заболеванием, значительно снижается у пожилых людей.

В журнале Annals of Neurology исследователи из Вашингтонского Университета в Сент-Луисе, штат Миссури, описали, как они обнаружили, что мозгу пожилых людей требуется гораздо больше времени, чтобы вывести бета-амилоид 42, основной ингредиент белковых бляшек, которые накапливаются в головном мозге при болезни Альцгеймера.
Рэндалл Дж. Бейтман, старший автор и профессор неврологии, сказал: «Мы обнаружили, что людям в 30 лет обычно требуется около 4 часов, чтобы вывести половину бета-амилоида 42 из головного мозга. В этом новом исследовании, мы показали, что в возрасте 80 лет этот процесс занимает больше 10 часов».
Если его не вывести, существует больше шансов, что бета-амилоид 42 – фрагмент белка, который является естественным побочным продуктом деятельности мозга – будет свертываться в бляшки, которые нарушают функции головного мозга, такие как коммуникация между клетками.
Ученые давно подозревали, что эти бляшки являются одним из главных факторов болезни Альцгеймера – формы деменции (слабоумия).
Деменция является прогрессирующим заболеванием, при котором память, мышление и поведение ухудшаются до тех пор, пока пациент больше не может поддерживать разговор и ухаживать за собой. Хотя эта болезнь поражает, в основном, пожилых людей, это не является нормальной составляющей старения.
По данным Всемирной организации здравоохранения, примерно 48 миллионов людей в мире страдают деменцией, и эта цифра растет почти на 8 миллионов каждый год. Болезнь Альцгеймера составляет примерно две третьих этих случаев.
Более низкие значения выведения бета-амилоида 42 у людей с симптомами болезни Альцгеймера
В своем исследовании профессор Бейтман и его коллеги протестировали 100 добровольцев в возрасте от 60 до 87 лет. У половины из этих участников наблюдались клинические признаки болезни Альцгеймера, такие как проблемы с памятью, а 62 участника имели формирование бляшек в головном мозге.
Исследователи установили наличие этих признаков и симптомов во время детального психического и физического обследования, которое прошли участники. Кроме сканирования головного мозга для обследования на наличие бляшек, ученые протестировали спинномозговую жидкость участников, используя технологию, которую они разработали самостоятельно.
При помощи этой технологии – названной SILK (stable isotope-linked kinetics – стабильная кинетика, связанная с изотопами) – исследователи смогли наблюдать, что происходит с бета-амилоидом 42 и другими белками.
У участников, в которых наблюдались свидетельства наличия бляшек, ученые обнаружили, что бета-амилоид 42 был более склонен к выходу из жидкости, омывающей головной мозг, и накапливанию в бляшках.
Кроме того, более низкие темпы выведения бета-амилоида 42 – такие как те, что исследователи увидели у пожилых участников – были связаны с симптомами болезни Альцгеймера, включая ухудшение памяти, изменения личности и деменцию.
Профессор Бейтман говорит, что ученые считают, что головной мозг имеет четыре способа утилизации бета-амилоида: перемещение его в спинной мозг, перемещение через гематоэнцефалический барьер, растворение или поглощение с другими белками, отложение в виде бляшек. Он приходит к выводу:
«При помощи дополнительных исследований, таких как это, мы надеемся определить, какой из первых трех способов утилизации бета-амилоида замедляется со старением головного мозга. Это может помочь нам в попытках разработки новых методов лечения».
К кому обратится:
Последнее изменение: 2020-01-16
Дата написания: 2015-08-10
Открытие о белке головного мозга стало причиной переосмысления развития болезни Альцгеймера
Алюминий в пище разрушает наш мозг?
Дорогие друзья. Статья не является медицинским советом и не может служить заменой консультации с врачом.
Источник
Амилоидные бляшки при болезни Альцгеймера – «уборка» биологического мусора?
Один из главных признаков болезни Альцгеймера – накопление в тканях головного мозга амилоидных бляшек из патологического белка, что считается основной причиной развития заболевания. Однако методы, нацеленные на избавление от них, раз за разом терпят неудачу в клинических испытаниях. Недавнее исследование не только объясняет возможную причину неудач антиамилоидной терапии, но и в корне меняет взгляды на образование плотных скоплений патологического белка
При болезни Альцгеймера – нейродегенеративном заболевании, развивающимся преимущественно в пожилом возрасте, – человек теряет память, у него ухудшается мышление, изменяется поведение. Итог – развитие старческого слабоумия. И на фоне роста продолжительности жизни благодаря достижениям медицины эта болезнь, как и другие возрастные заболевания, встречается все чаще: по прогнозам, к 2050 г. число таких больных в мире достигнет 100 млн.
Почему болезнь Альцгеймера до сих пор является неизлечимой? Еще четверть века назад была предложена амилоидная гипотеза развития этого заболевания, связанная с отложением в тканях мозга белка бета-амилоида. Амилоидные бляшки могут быть разных типов, самые распространенные – диффузные, представляющие собой слабо организованные аморфные «облака», а также плотные, с компактным центром.
Последние служат объектами особого внимания ученых: было сделано несколько попыток создать лекарство от болезни Альцгеймера на основе моноклональных антител, способных снижать численность плотных амилоидных бляшек, но результаты клинических испытаний были как минимум неоднозначны.
Считается, что оба типа амилоидных бляшек образуются в мозге спонтанно, а уничтожают их клетки микроглии – иммунные клетки мозга. Микроглия должна работать, как и другие макрофаги: эти клетки имеют белки-рецепторы семейства ТАМ, с помощью которых они распознают, а затем «съедают» отжившую свое клетку. При этом клетка, подлежащая уничтожению, должна сигнализировать об этом определенной молекулой на поверхности – «сигналом смерти».
Именно такой молекулярный сигнал присущ и амилоидным образованиям. Недавно ученые из Института биологических исследований Солка (США) с использованием лабораторных мышей, служащих моделью болезни Альцгеймера, выяснили, что клетки микроглии, несущие рецепторы ТАМ, способны поглощать диффузный бета-амилоид. Внутри этих клеток поглощенные белковые фибриллы уплотняются, и именно из них формируется плотная бляшка.
По мнению исследователей, речь идет о защитном механизме, с помощью которого происходит структурная «организация» более опасного для нейронов диффузного бета-амилоида, в результате чего межклеточное пространство очищается от этого «мусора». Более того, они предполагают, что увеличение активности рецепторов ТАМ в клетках микроглии и связанное с этим ускорение образования плотных бляшек помогает смягчить симптомы болезни Альцгеймера. Эту гипотезу ученые планируют проверить экспериментально.
В заключение авторы предлагают перестать искать способы разрушения амилоидных бляшек, а заняться методами, которые позволят уменьшить синтез патологического белка либо улучшить его выведение из тканей мозга.
Источник
Клинические рекомендации по диагностике и лечению системного амилоидоза
В клинических рекомендациях, подготовленных специалистами различного профиля, рассматриваются методы диагностики и лечениясистемного амилоидоза, в том числе АА (вто-ричный амилоидоз при хронических воспалительных заболеваниях, включая ревматоидныйартрит, анкилозирующий спондилит, аутовоспалительные заболевания, хроническиенагноения, злокачественные опухоли и др.), AL (амилоидоз при плазмоклеточных дискразиях – идиопатический, при миеломной болезни и макроглобулинемии Вальденстрема) иATTR (транстиретиновый; семейные формыполиневропатического, кардиопатического идругого амилоидоза, системный старческийамилоидоз). Диагноз амилоидоза, которыйможно заподозрить на основании клиническихданных, необходимо подтвердить при гистологическом исследовании (окрашивание препаратов ткани конго-красным с последующей микроскопией в поляризованном свете). Чтобы замедлить или приостановить прогрессирование амилоидоза любого типа, необходимо добиться уменьшения количества (или, если возможно, удаления) белков-предшественников путем лечения хронического воспаленияпри АА-амилоидозе или подавления пролиферации клона плазматических клеток для уменьшения продукции легких цепей иммуно-глобулинов при AL-амилоидозе. Для замедления прогресирования ATTR-амилоидоза упациентов с полиневропатией применяют тафамидис, который ингибирует диссоциацию мутантного транстиретина и снижает его амилоидогенность.
Определение, классификация, группы риска и принципы диагностики
Амилоидоз – группа заболеваний, отличительным признаком которых является отложение в тканях и органах фибриллярного гликопротеида амилоида. Специфическое свойство амилоида, отличающее его от других фибриллярных белков стромы, – способность к двойному лучепреломлению, что проявляется свечением в поляризованном свете предварительно окрашенных конгокрасным препаратов амилоида с изменением красного цвета конгофильных амилоидных отложений на яблочно-зеленый (дихроизм).
В основе амилоидогенеза лежит синтез большого количества нестабильных белковпредшественников, которые агрегируются с образованием амилоидной фибриллы. Клю чевое значение имеет амилоидогенность основного белка-предшественника амилоида, специфичного для каждой формы амилоидоза (в настоящее время известно более 30 таких белков), обозначение которого положено в основу современной классификации заболевания (ВОЗ, 2016 г.). Названия типов амилоида включают в себя букву А, означающую “амилоид», и обозначение конкретного фибриллярного белка амилоида – А (амилоидный А-протеин), L (легкие цепи иммуноглобулинов), TTR (транстиретин), β2М (β2-микроглобулин), В (В-протеин), IAPP (островковый амилоидный полипептид). Используют также производные наименования – иммуноглобулиновый амилоидоз (AL), транстиретиновый (ATTR) и др. (табл. 1) 2. Следует отметить, что Международная классификация болезней (МКБ) 10-го пересмотра базируется на клиническом принципе, не учитывает особенности патогенеза различных форм амилоидоза и не позволяет обосновать адекватное лечение.
| Белок амилоида | Белок-Белок-предшественник | Клиническая форма амилоидоза |
|---|---|---|
| АА | SSA-белок | Вторичный амилоидоз при хронических воспалительных заболеваниях, в том числе периодической болезни и синдроме Макла-Уэллса |
| AL | λ, κ-легкие цепи иммуноглобулинов | Амилоидоз при плазмоклеточных дискразиях – идиопатический, при миеломной болезни и макроглобулинемии Вальденстрема |
| ATTR | Транстиретин | Семейные формы полиневропатического, кардиопатического и др. амилоидоза, системный старческий амилоидоз |
| Аβ2М | β2-микроглобулин | Диализный амилоидоз |
| AGel | Гелсолин | Финская семейная амилоидная полиневропатия |
| AApoAI | Аполипопротеин А-I | Амилоидная полиневропатия (III тип по van Allen, 1956 г.) |
| AFib | Фибриноген | Амилоидная нефропатия |
| Aβ2 | β-белок | Болезнь Альцгеймера, синдром Дауна, наследственные кровоизлияния в мозг с амилоидозом |
| APrPScr | Прионовый белок | Болезнь Крейтцфельда-Якоба, болезнь Герстманна-Штраусслера-Шейнкера |
| AANF | Предсердный натрийуретический фактор | Изолированный амилоидоз предсердий |
| AIAPP | Амилин | Изолированный амилоидоз в островках Лангерганса при сахарном диабете 2 типа, инсулиноме |
| ACal | Прокальцитонин | При медуллярном раке щитовидной железы |
| ACys | Цистатин С | Наследственные кровоизлияния в мозг с амилоидозом (Исландия) |
АА-амилоидоз чаще всего развивается при ревматоидном артрите, серонегативных спондилоартропатиях, аутовоспалительных наследственных периодических лихорадках, в том числе периодической болезни (семейной средиземноморской лихорадке), а также при хронических нагноениях, туберкулезе. АА-амилоид образуется из сывороточного предшественника SAA (serum amyloid A) – острофазового белка, продуцируемого в значительных количествах в ответ на воспаление. По этой причине АА-амилоидоз называют также реактивным или вторичным.
Клинические формы AL-амилоидоза обусловлены единым этиологическим фактором – В-лимфоцитарной дискразией, характеризующейся формированием аномального клона плазматических или В-клеток в костном мозге, которые продуцируют аномальные иммуноглобулины, обладающие амилоидогенностью (легкие цепи моноклонального иммуноглобулина, чаще λ, реже κ-типа). При первичном AL-амилоидозе плазмоклеточная дискразия относительно более доброкачественная, в то время как при В-гемобластозах (множественной миеломе, болезни Вальденстрема и др.) она обладает признаками злокачественной опухоли. Аномальный амилоидогенный клон плазматических клеток может формироваться также из плазмоцитов, локализующихся вне костного мозга, что может привести к развитию локального амилоидоза. Наиболее распространенные локальные формы AL-амилоидоза – амилоидоз трахеи, бронхов и гортани, мочевого пузыря. Выявление плазмоклеточной дискразии необходимо для диагностики AL-амилоидоза, а также для оценки его риска и дифференциального диагноза.
ATTR-амилоидоз является необратимо прогрессирующим заболеванием с высокой степенью инвалидизации вследствие тяжелого поражения сердца, периферической и/или автономной полиневропатии. Пациенты обычно умирают в течение 10-12 лет от первых проявлений. Развитие ATTR-амилоидоза обусловлено мутациями в молекуле транстиретина или возрастным нарушением секреции тетрамеров транстиретина печенью. В обоих случаях происходит распад тетрамеров транстиретина до мономеров, обладающих выраженной конформационной нестабильностью.
Рекомендации:
- Скрининг АА-амилоидоза следует проводить в следующих группах риска: серопозитивные и серонегативные хронические полиартриты (ревматоидный артрит, анкилозирующий спондилоартрит, ювенильный хронический артрит, псориатический артрит, синдром Рейтера и др.), воспалительные заболевания кишечника (болезнь Крона, язвенный колит), аутовоспалительные заболевания (подагра тяжелого рецидивирующего течения, семейные периодические лихорадки – периодическая болезнь, криопиринопатии, TRAPS, гипериммуно глобулинемия D), хронические нагноения (туберкулез, бронхоэктатическая болезнь, остеомиелит и др.), злокачественные солидные опухоли [1,2,4-6].
- Риск АА-амилоидоза у больных с хроническими воспалительными заболеваниями повышается при персистирующем увеличении уровней маркеров острой фазы воспаления (С-реактивный белок, SAA), наличии анемии хронических заболеваний (с повышением уровня ферритина крови), особенно в сочетании с суставным синдромом (синовитом) [4,6-12]. Дина мический контроль за уровнем этих показателей необходим также при мониторировании течения диагностированного АА-амилоидоза. Для оценки риска развития или прогрессирования АА-амилоидоза в условиях преимущественного аутовоспаления или с целью выявления субклинической активации воспаления можно определять сывороточный маркер нейтрофильной активности S100A12 (кальгранулин) [4,13-15].
- Диагностика аутовоспалительных заболеваний предполагает, в первую очередь, проведение генетического исследования на мутации генов MEFV (пирин), NLRP3 (криопирин), TRAPS (рецептор к фактору некроза опухоли альфа), мевалонаткиназы [4,16-25].
- Высокая частота олигосекреторных моноклональных гаммапатий у лиц старше 50 лет требует скринингового обследования этой группы лиц на предмет моноклональных гаммапатий. Наиболее чувствительным и недорогим турбидиметрическим методом для скрининговой диагностики являет Freelite-метод количественной оценки уровня свободных легких цепей иммуноглобулинов. Все больные с плазмоклеточными дискразиями и лимфопролиферативными заболеваниями входят в группу риска AL-амилоидоза 28.
- У пациентов с морфологически подтвержденным амилоидозом диагностика AL-амилоидоза предполагает проведение иммунохимического исследования с применением высокочувствительных методов – иммунофиксации сыворотки и суточной мочи, количественного определения свободных легких цепей иммуноглобулинов (Freelite) 30.
- Помимо выявления моноклональной гаммапатии, диагностика плазмоклеточной дискразии предполагает выявление и оценку количества плазмоцитов костного мозга, а также их структурных особенностей. Применение цитогенетического исследования и иммунофенотипирования плазмоцитов важно для уточнения клональности и злокачественности аберрантного клона плазматических клеток, в особенности в редких случаях неинформативности иммунохимического исследования крови и суточной мочи [26,33-34,36,37].
- Важное значение в диагностике плазмоклеточных дискразий имеют также иммуногистохимические методы выявления патологического клона плазматических клеток. Это особенно важно для диагностики, типирования и лечения локального варианта ALамилоидоза [35].
- ATTR-амилоидоз следует подозревать у пациентов с полиневропатией, необъяснимым чередованием запоров и диареи, синдромом карпального канала, особенно при наличии полиневропатии, синдрома карпального канала, кардиомиопатии у родственников. Важными симптомами являются геморрагии, фестончатый край зрачка, потеря массы тела, снижение зрения 40.
- Диагностика амилоидоза основывается на результатах морфологического исследования [1-2,39,48].
- При системном амилоидозе для диагностики амилоидного поражения органа нет необходимости проводить его биопсию у больных с ранее верифицированным диагнозом амилоидоза по результатам биопсии другого органа. Однако точная диагностика возможна только с помощью морфологического исследования [1,48].
- С целью выявления амилоида необходимо окрашивание препаратов ткани красителем конго-красный с последующей микроскопией в поляризованном свете. Окончательный диагноз амилоидоза устанавливают при выявлении конгофильных масс, обладающих способностью к яблочно-зеленому или желтоватому свечению в поляризованном свете [1,39,48]. Для более точной диагностики амилоидоза применяют также метод окраски тиофлафином Т, который дает светло-зеленое свечение амилоида [1,2].
- При системном амилоидозе информативна биопсия прямой или двенадцатиперстной кишки (с захватом подслизистого слоя). ATTR-амилоид отличается слабой конгофилией. По этой причине выявить этот тип амилоида нередко удается только при повторных биопсиях из разных органов – аспирационной биопсии подкожной жировой клетчатки, биопсии слюнных желез губ и др. Наиболее эффективна биопсия пораженного органа [1-2,39,48]. У пациентов с синдромом запястного канала исследованию на амилоид необходимо подвергать ткань, удаленную при оперативной декомпрессии запястного канала.
- Не рекомендуется проводить биопсию подкожной жировой клетчатки у больных инсулинозависимым сахарным диабетом, так как в местах иньекций инсулин может агрегировать и формировать амилоидные депозиты [48].
- Для дифференциальной диагностики АА-амилоидоза от AL- и ATTR-амилоидоза используют окрасочные методы при тщательном учете клинических предпосылок разных типов амилоидоза [48,49].
- Наиболее эффективным методом типирования является иммуногистохимическое исследование. Поскольку некоторые антисыворотки могут давать перекрестные реакции с разными типами амилоида, исследование целесообразно проводить с панелью антисывороток. Для неспециализированных терапевтических и нефрологических стационаров рекомендуется применение панели антисывороток к SAA, разным типам тяжелых цепей иммуноглобулинов, легким цепям иммуноглобулинов λ и κ, транстиретину. Важно также использовать антисыворотки к фибриногену [36,50].
- Для диагностики ATTR-амилоидоза необходимо генетическое исследование на наличие мутации гена транстиретина [39].
Клинические проявления
Для вторичного АА-амилоидоза характерно более раннее начало, чем для AL-амилоидоза (средний возраст больных составляет около 40 и 65 лет, соответственно). ATTR-амилоидоз, несмотря на наследственную природу, характеризуется низкой пенетрантностью и также проявляется обычно после 35 лет.
Поражение почек – ведущий клинический признак АА- и AL-амилоидоза, наблюдающийся практически у всех больных. Поражение почек встречается и у больных с многими формами семейного амилоидоза (AFib, ALys, AGel и др.). При ATTR-амилоидозе нефропатия отмечается лишь у 20-23% больных. Клинически амилоидная нефропатия характеризуется неуклонно прогрессирующим течением с последовательной сменой стадий: протеинурия, нефротический синдром, хроническая почечная недостаточность (ХПН). Иногда возможно развитие ХПН без предшествующего нефротического синдрома.
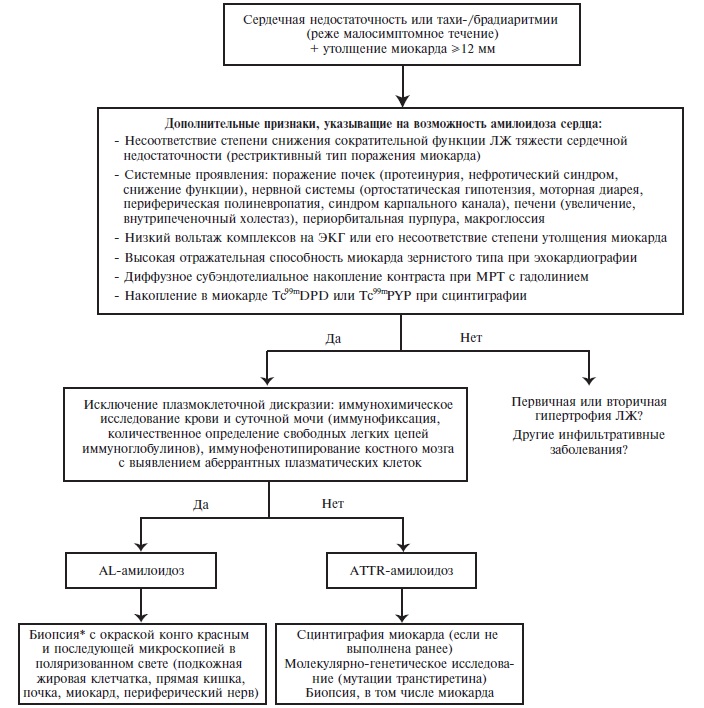
Поражение сердца развивается у подавляющего большинства больных AL-амилоидозом и у 50-60% пациентов с АTTR-амилоидозом, но не характерно для АА-амилоидоза (рис. 1). При эхокардиографии у больных амилоидозом сердца наблюдается утолщение межжелудочковой перегородки и стенки левого желудочка (чаще симметричное), которое не сопровождается электрокардиографическими признаками гипертрофии миокарда. У части больных отмечается снижение вольтажа зубцов на ЭКГ, хотя отсутствие этого признака не исключает диагноз амилоидоза сердца. Нарушение диастолической функции левого желудочка (рестриктивный тип) приводит к развитию сердечной недостаточности, которая быстро прогрессирует, плохо поддается лечению и почти у 50% пациентов оказывается причиной смерти. Кроме того, у больных амилоидозом сердца часто наблюдаются различные аритмии и нарушения проводимости.
При AL-амилоидозе и особенно ATTR-амилоидозе часто встречается ортостатическая артериальная гипотензия – вариант сосудистой недостаточности, при которой сосуды теряют способность поддерживать нормальное артериальное давление в условиях ортостатических нагрузок. Она проявляется ощущением дурноты и потемнением в глазах в ортостазе в сочетании с резким снижением АД. Обычно этот симптом связан с дисфункцией автономной нервной системы (амилоидоз нервных сплетений сосудов). Тяжелая ортостатическая гипотензия сопровождается обмороками, а иногда приводит к развитию острого нарушения мозгового кровообращения.
Поражение желудочно-кишечного тракта может проявляться, особенно при AL-амилоидозе, тяжелой диареей или динамической непроходимостью, которые чаще связаны с нарушениями моторики кишечника вследствие дисфункции автономных нервных сплетений. Иногда выявляют изъязвления или перфорацию стенок с возможным кровотечением. При поражении пищевода возможна дисфагия.
Поражение печени при АА- и AL-типах амилоидоза наблюдают практически в 100% случаев. Функция печени чаще остается сохранной, редким признаком амилоидоза печени является внутрипеченочная портальная гипертензия. При некоторых вариантах семейного ALys-амилоидоза описаны тяжелые спонтанные внутрипеченочные кровотечения.
Увеличение селезенки, обусловленное амилоидным поражением, отмечается у большинства больных и обычно сопутствует увеличению печени.
Поражение нервной системы, представленное симптомами периферической соматической и автономной невропатии, отмечают у 17-35% больных AL-амилоидозом и практически у всех пациентов с наследственной амилоидной полиневропатией разных типов (ATTR, AApoA1 и др.). В большинстве случаев развивается дистальная симметричная полиневропатия с неуклонно прогрессирующим течением, различные дисфункции автономной нервной системы. Реже выявляют двусторонний синдром запястного канала, обусловленный сдавлением срединного нерва депозитами амилоида.
Поражение кожи наблюдают почти у 40% больных AL-амилоидозом. Помимо параорбитальных геморрагий описаны также папулы, бляшки, узелки, пузырьковые высыпания, склеродермоподобная индурация кожи.
Амилоидные отложения в мышцах чаще встречаются при AL-амилоидозе. Макроглоссия – патогномоничный симптом AL-амилоидоза, развивающийся примерно у 20% пациентов.
Редким проявлением амилоидоза, описанным при AL- и, в особенности, АTTR-типах, бывает поражение глаз (сухой кератоконъюнктивит, вторичная глаукома, помутнение стекловидного тела, дисфункции зрачка).
Клиническая картина других типов амилоидоза варьируется в зависимости от основной локализации и распространенности амилоидных депозитов, которые иногда могут быть значительными и напоминать проявления AL-амилоидоза.
Рекомендации:
- Наиболее типичное проявление амилоидоза почек – изолированная протеинурия более 0,5 г/сут, чаще нефротического уровня. Иногда при множественной миеломе важное значение приобретает иммунохимическое электрофоретическое исследование мочи для отличия альбуминурии в рамках амилоидоза и протеинурии переполнения (наличие в моче белка БенсДжонса, реакция термопреципитации белка Бенс-Джонса не обладает достаточной информативностью). Для установления связи протеинурии с амилоидозом необходимо также исключить протеинурию, связанную с диабетической нефропатией и гипертонической почкой [4,5,29,48,51-56].
- На амилоидоз сердца указывает утолщение межжелудочковой перегородки и/или задней стенки левого желудочка более 12 мм при эхокардиографии, особенно в сочетании с низкоамплитудной ЭКГ. Дифференциальный диагноз проводят с гипертрофией левого желудочка, которая может быть следствием артериальной гипертонии, аортальных пороков, гипертрофической кардиомиопатии и других причин [29,37-39,42,48,51-53,57-62].
- Характерное проявление амилоидоза сердца – низкая амплитуда желудочковых комплексов на ЭКГ (менее 5 мм в отведениях от конечностей). Пато логические Q-зубцы у больных амилоидозом нередко являются псевдоинфарктными (вследствие электрически нейтральных отложений амилоида, имитирующих рубцовые изменения), однако при амилоидозе коронарных артерий возможно развитие и истинного инфаркта миокарда [29,37-39,42,48,51-53,56-62].
- При амилоидозе сердца наблюдается рестриктивное нарушение диастолической функции левого желудочка, фракция выброса часто остается нормальной, или степень ее снижения не соответствует тяжести сердечной недостаточности [29,37-39,42,48,51-53,5662].
- Всем больным с амилоидозом сердца необходимо проведение стандартной эхокардиографии с допплерометрической оценкой трансмитрального крово тока, при наличии технической возможности оправдано также проведение тканевой допплерометрии миокарда для более точной оценки внутрисердечной гемодинамики. В стандарт обследования больных амилоидозом сердца входят также ЭКГ и суточное мониторирование АД и ЭКГ [1,2,29,37-39,42,48,5153,56-62].
- Магнитно-резонансная томография (МРТ) с контрастированием гадолинием с высокой вероятностью выявляет инфильтративный характер поражения миокарда и имеет особое диагностическое значение при “изолированном» поражении сердца [48,56,6062].
- Амилоидную инфильтрацию сердца позволяет выявить также сцинтиграфия миокарда с пирофосфатом технеция, особенно при наличии трудностей в морфологической диагностике ATTR-амилоидоза, для которого характерна слабая конгофилия пораженных тканей. Интенсивное накопление радиоактивного препарата в миокарде (2+/3+) в сочетании с утолщением миокарда неясной этиологии указывает на высоко вероятный ATTR-амилоидоз, если у пациента исключен диагноз AL-амилоидоза (рис. 1) [39,42,58-59,62].
- Диагноз амилоидоза сердца может быть подтвержден при биопсии миокарда. Однако проведение этого исследования обычно не требуется при наличии типичных эхокардиографических изменений у пациентов с амилоидозом, установленным при биопсии другого органа, например, почки или слизистой оболочки прямой или двенадцатиперстной кишки.
- Диагностика периферической амилоидной полиневропатии основывается на клинической оценке неврологических проявлений: обычно выявляют различные нарушения чувствительности, в частности температурной и болевой. Из-за поражения преимущественно мелких немиелинизированных волокон электромиография и исследование скорости проведения нервного импульса обычно неинформативны для ранней диагностики амилоидной полиневропатии [38,39]. Доминирование жалоб, связанных с поражением нервной системы, является отличительной чертой ATTR-амилоидоза.
- Электромиография наряду с другими нейрофизиологическими методами (количественное сенсорное тестирование, конфокальная микроскопия нервов роговицы, оценка состояния интраэпидермальных нервных волокон в биоптате кожи) может использоваться для оценки характера (признаки аксонального и/или аксонально-демиелинизирующего типа поражения двигательных и чувствительных волокон нервов конечностей) и тяжести неврологических нарушений. Электромиография в сочетании с ультразвуковым исследованием периферических нервов позволяет объективизировать их повреждение в анатомически узких каналах (туннельные невропатии) [38,39].
- Признаками I стадии амилоидной полиневропатии являются незначительные нарушения чувствительности по полиневропатическому типу, более выраженные в ногах, пациент сохраняет способность к самостоятельной ходьбе. При II стадии полиневропатии из-за нарастания чувствительных и присоединения двигательных нарушений в виде нижнего периферического преимущественно дистального парапареза походка пациента нарушается, требуется опора на трость или костыли. На III стадии тяжелые двигательные нарушения приковывают пациента к постели, передвижение возможно только на инвалидной коляске [38,39,46].
- Поражение вегетативной нервной системы чаще всего проявляется ортостатической гипотензией разной степени тяжести. Однако систолическое артериальное давление менее 90 мм рт. ст. может быть обусловлено низким сердечным выбросом у больных с сердечной недостаточностью или гиповолемией при тяжелом нефротическом синдроме. Другие частые проявления поражения вегетативной нервной системы – моторная диарея, дисфункция мочевого пузыря, половой сферы, гипогидроз [1,2,38,51]. Наряду с моторной диареей причиной значительного (на 9-18 кг) снижения массы тела могут быть нарушения трофики мышц [38,39].
- Двусторонний синдром запястного канала наиболее характерен для ATTR-, β2М- и AL-амилоидоза и проявляется интенсивными болями и парестезиями в IIII пальцах кистей с постепенной атрофией мышц тенара [38,39].
- МРТ головного мозга с контрастным усилением проводят при наличии клинических признаков поражения центральной нервной системы [38,39].
- Основным признаком амилоидоза печени является ее увеличение, наиболее специфична гепатомегалия более 15 см по данным компьютерной томографии. У больных амилоидозом печени обычно выявляют также холестаз (повышение активности щелочной фосфатазы и/или g-глютамилтранспептидазы в 1,5 раза по сравнению с верхней границей нормы). Ложная диагностика амилоидоза печени возможна у больных с тяжелой застойной правожелудочковой недостаточностью [2,4,48,51].
- Для выявления амилоидоза печени, селезенки и почек всем пациентам проводят ультразвуковое исследование этих органов, в некоторых случаях необходимо проведение компьютерной томографии брюшной полости [2,48].
- Диарея вследствие инфильтрации амилоидом стенки желудочно-кишечного тракта возникает редко, такую диарею трудно дифференцировать от моторной диареи в рамках поражения вегетативной нервной системы. Наиболее надежно вовлечение желудочнокишечного тракта при амилоидозе устанавливают по результатам морфологического исследования. Одна ко обнаружение амилоида только в стенках сосудов желудочно-кишечного тракте не является критерием его поражения, необходимо обнаружение амилоидных депозитов в интерстиции подслизистого слоя кишечника [1-2,5,48,52].
- Нодулярный легочный и трахеобронхиальный амилоидоз за редким исключением – это проявление локального AL-амилоидоза. Для системного AL-амилоидоза характерно обнаружение диффузного интерстициального легочного амилоидоза. В связи с редкостью дыхательной недостаточности необходимости в морфологической верификации легочного амилоидоза обычно не возникает. Наиболее информативным методом диагностики амилоидоза легких является компьютерная томография [1,2,48]. У больных локальным трахеобронхиальным AL-амилоидозом важными методами мониторирования течения заболевания являются ларингоскопия и бронхоскопия [27,48].
- На амилоидоз плевры указывает рецидивирующий плевральный выпот, который не зависит от эффективности лечения отечного синдрома, обусловленного сердечной недостаточностью или нефротическим синдромом. При амилоидном поражении плевры жидкость, полученная во время пункции плевральной полости, нередко содержит примесь крови. При амилоидозе плевры эвакуация плеврального выпота, как правило, малоэффективна из-за быстрого его накопления [1,2,48].
- Поражение мягких тканей характерно для AL-амилоидоза. Макроглоссия с инфильтрацией дна ротовой полости и периорбитальная пурпура (и кожные геморрагии на теле) патогномоничны для этого типа амилоидоза. Возможны также псевдогипертрофия скелетных мышц с развитием мышечной слабости, лимфаденопатия, амилоидоз височной артерии [1,2,39,48,52].
- Признаками прогрессирования амилоидоза сердца являются дальнейшее утолщение миокарда (на 2 мм и более), увеличение функционального класса сердечной недостаточности, снижение фракции выброса левого желудочка на 10% и более. Показатели тяжести амилоидоза сердца – увеличение уровня NTproBNP (особенно более 1800 нг/л) и тропонинов (тропонин Т более 0,025 нг/мл). Критериями прогрессирования амилоидоза почек считают увеличение протеинурии (на 50% от исходного уровня, как правило на 1 г/сут и более) и сывороточного уровня креатинина (на 25% и более от исходного). Информативным критерием прогрессирования амилоидоза печени является увеличение активности щелочной фосфатазы на 50% от исходной. Прогрес сирование полиневропатии объективизируют на основании результатов стимуляционной электромиографии и других нейрофизиологических и нейровизуализационных методов обследования (см. выше). Важным показателем тяжести больных AL-амилоидозом является разница в содержании свободных легких цепей иммуноглобулинов более 180 мг/л, установленная методом Freelite [2,38,51,48,60,61,64].
Лечение системного амилоидоза
Целью терапии любого типа амилоидоза служит уменьшение количества (или, если возможно, удаление) белков-предшественников для того, чтобы замедлить или приостановить прогрессирование болезни. Неблаго приятный прогноз при естественном течении амилоидоза оправдывает применение агрессивных методов лечения. Клиническое улучшение, достигаемое с помощью лечения, включает стабилизацию или восстановление функции жизненно важных органов, а также предотвращение функциональных нарушений с увеличением продолжительности жизни больных. Лечение амилоидоза должно включать симптоматические методы, направленные на уменьшение выраженности сердечной недостаточности, аритмии, отечного синдрома, коррекцию артериальной гипотензии и др.
Лечение АА-амилоидоза
Цель терапии АА-амилоидоза – подавление продукции белка-предшественника SAA (вплоть до устойчивой нормализации), что достигается активным лечением хронического воспаления (в том числе субклинического). Это позволяет уменьшить клинические проявления и предотвратить прогрессирование амилоидной нефропатии и существенно улучшить прогноз.
Рекомендации:
- Основной стратегией лечения АА-амилоидоза является эффективное подавление воспаления. Лечение должно проводиться вне зависимости от клинической активности воспалительного заболевания до нормализации уровня маркеров острой фазы воспаления – С-реактивного белка (предпочтительно применение высокочувствительного метода измерения) и/или SAA [10-13,63,66-77].
- Больным ревматоидным артритом и серонегативными спондилоартропатиями необходима постоянная пожизненная базисная терапия. Предпочтение отдают генно-инженерным биологическим препаратам, в том числе ингибиторам фактора некроза опухоли-α, интерлейкина-6, ритуксимабу. После оценки эффективности и безопасности базисной терапии оправдано присоединение терапии колхицином в дозе 2 мг/сут [10-13,63,66-77].
- Препаратом выбора при периодической болезни и тяжелой рецидивирующей подагре является колхицин в дозе 2 мг/сут. Начальная доза препарата составляет 0,5 мг/сут, затем ее постепенно увеличивают до целевой под контролем клинического анализа крови и сывороточного уровня креатинина. Для предупреждения осмотической диареи, обусловленной колхицином, возможно временное назначение ферментных препаратов. Дозу колхицина снижают до 1 мг/сут у больных с хронической болезнью почек 4-5 стадии [1,2,4,69]. При неэффективности колхицина показано назначение ингибиторов интерлейкина-1, в частности канакинумаба.
- При криопиринопатиях, TRAPS препаратами выбора являются ингибиторы интерлейкина-1, к которым присоединяют колхицин [18,19,74-77].
- При хронических нагноениях важное значение имеет хирургическое лечение. В дальнейшем или одновременно проводят лечение димексидом (5-10 г/сут в разведении большим количеством соков – томатного, гранатового и др.). Препарат предпочтителен при легочных нагноениях [1-2,4,6,31].
Лечение АL-амилоидоза
При AL-амилоидозе, как и при множественной миеломе, целью лечения служит подавление пролиферации клона плазматических клеток для уменьшения продукции легких цепей иммуноглобулинов. В отличие от множественной миеломы, принципиальной задачей лечения AL-амилоидоза является по возможности полная элиминация патологического клона. В связи с быстрым прогрессированием заболевания важное значение имеет применение быстродействующих схем лечения на основе бортезомиба. По мере достижения ремиссии у некоторых больных применяют высокодозную химиотерапию с поддержкой аутологичными стволовыми клетками. При строгом подборе больных с исключением противопоказаний к этой терапии эффект достигают у 60% больных. У больных с клиническими симптомами амилоидоза сердца, ортостатической гипотензией, диареей, желудочно-кишечными кровотечениями в анамнезе, а также у лиц старше 70 лет с амилоидным поражением двух и более систем организма проведение высокодозной химиотерапии не рекомендуется. Тяжелый агранулоцитоз и другие осложнения существенно ограничивают ее применение. Проводят также лечение талидомидом или леналидомидом. Колхицин при AL-амилоидозе не эффективен.
Рекомендации:
- Основной стратегией лечения АL-амилоидоза является элиминация амилоидогенного клона плазматических клеток костного мозга. После достижения гематологической ремиссии проводят противорецидивное лечение в течение не менее 12 месяцев. В этот период при отсутствии противопоказаний возможна высокодозная химиотерапия с поддержкой аутологичными стволовыми клетками, которая позволяет достичь длительной ремиссии [2,26,37,56,57,65,78,79].
- Полный гематологический ответ диагностируют на основании исчезновения моноклональных амилоидогенных иммуноглобулинов по данным иммунофиксации крови и суточной мочи, количественного определения свободных легких цепей иммуноглобулинов методом Freelite (нормальный уровень легких цепей κ – менее 19,4 мг/л, λ – менее 26,3 мг/л, нормальное соотношение легких цепей в пределах 0,261,65). При снижении уровня свободных легких цепей на 50% от исходного диагностируют частичный ответ, критерием очень хорошего частичного ответа является разница между содержанием двух типов легких цепей иммуноглобулинов менее 40 мг/л [37,60,61,64].
- Клинический эффект терапии в первую очередь оценивают по динамике кардиологических и ренальных показателей. Особо выделяют NT-proBNP-ответ (снижение уровня маркера на 30% и более или на 300 нг/л и более у пациентов с исходным уровнем более 650 нг/л). С клиническим эффектом лечения больше коррелирует почечный ответ (снижение протеинурии на 75% и более, повышение сывороточного креатинина не более 25% от исходного). Ответ со стороны других органов не обладает существенной прогностической информативностью. Эффективность лечения амилоидоза печени оценивают по снижению активности щелочной фосфатазы (на 50% и более) и уменьшению размеров печени (краниокаудальный размер по данным КТ должен уменьшиться на 30% в течение года после достижения гематологической ремиссии). Эффективность лечения амилоидной полиневропатии определяют, главным образом, по результатам клинического неврологического осмот ра. Уменьшение амилоидных депозитов в мягких тканях может быть оценено по данным компьютерной томографии или МРТ. Эффективным методом оценки общего содержания амилоида в тканях служит сцинтиграфия с радиоактивным амилоидным Ркомпонентом [2,26,37,57,60,61,64].
- Учитывая возможность достижения быстрого гематологического ответа, терапией первой линии, особенно у больных с высоким риском быстрого прогрессирования, считают комбинированные схемы на основе бортезомиба, например, трехкомпонентная схема: бортезомиб 1,3 мг/м2 внутривенно или подкожно (1, 5, 8 и 11-й дни цикла), мелфалан 0,15 мг/кг внутрь (с 1-го по 4-й день) и дексаметазон 20 мг/сут внутрь (1, 5, 8 и 11-й дни). Для большей безопасности предпочтительно подкожное введение бортезомиба. Если в дальнейшем планируется высокодозная химиотерапия с поддержкой аутологичными стволовыми клетками мелфалан в составе трехкомпонентной схемы заменяют на циклофосфамид (400 мг внутривенно капельно в 1, 8, 12-й дни), который не вызывает истощение пула стволовых клеток в костном мозге. Курсы химиотерапии на основе бортезомиба проводят каждые 4 недели (всего 8 курсов). Одновременно назначают омепразол, низкомолекулярные гепарины (для профилактики тромбозов при применении высоких доз дексаметазона), при наличии показаний – антибиотики, противогрибковые препараты, ацикловир [65,78,79].
- Не менее эффективна схема терапии мелфаланом (внутрь 0,15 мг/кг с 1-го по 4-й день) и дексаметазоном (внутрь 20 мг/сут в дни 1-4, 9-12 и 17-21) каждые 4-6 недель. Основным недостатком этой схемы является медленное формирование гематологического ответа, что делает ее менее перспективной у больных с высоким риском быстрого прогрессирования амилоидоза. Одновременно назначают омепразол, низкомолекулярные гепарины (для профилактики тромбозов при применении высоких доз дексаметазона), при наличии показаний – антибиотики, противогрибковые препараты, ацикловир [1,2,37,56,57,65,78,79].
- У тяжелых больных с декомпенсированной сердечной недостаточностью может применяться схема терапии мелфаланом (внутрь 0,15 мг/кг с 1-го по 4-й дни) и преднизолоном (0,8 мг/кг с 1-го по 7-й день). Однако эффективность этой схемы ограничена [1,2,56,57,65,78,79].
Лечение ATTR-амилоидоза
До недавнего времени единственным методом лечения ATTR-амилоидоза была трансплантация печени, секретирующей нормальный транстиретин. Поскольку 98% всего сывороточного транстиретина синтезируется печенью, это позволяло прервать продукцию мутантного транстиретина. Трансплантация печени существенно замедляет прогрессирование ATTR-амилоидоза, а 20летняя выживаемость больных после трансплантации составляла 55,3% [36]. Однако уже имеющиеся массы амилоида способны выступать в роли ядра нуклеации для новых депозитов амилоида на основе нормального транстиретина (амилоидускоряющая субстанция). В настоящее время у больных с ранними стадиями ATTRамилоидной полиневропатии апробированы консервативные методы стабилизации тетрамерной структуры мутантного транстиретина и, следовательно, подавления его амилоидогенности. Один из таких препаратов – тафамидис замедлял на 52% (р=0,027) прогрессиро вание неврологических нарушений у больных ATTRамилоидозом, сохраняя функцию периферических соматических и автономных нервных волокон [12]. В клиническом исследовании III фазы лечение тафамидисом по сравнению с плацебо у больных с ATTR-амилоидозом сердца вызывало снижение общей смертности и частоты госпитализаций по сердечно-сосудистым причинам и задерживало ухудшение функциональной активности [81]. В Российской Федерации применение тафамидиса зарегистрировано только для лечения ATTR-амилоидоза с периферической полиневропатией.
В качестве стабилизатора транстиретина изучается также дифлюнизал из группы нестероидных противовоспалительных препаратов, однако его эффективность показана только в экспериментальных условиях.
Источник