Сахарный диабет и здоровая печень
Задать вопрос
Ваше сообщение принято!
Печень … К этой части человеческого тела очень подходит эпитет «самый»: самый массивный внутренний орган, самая большая пищеварительная железа, самые разнообразные функции, самая способная к восстановлению … Но бывают ситуации, когда печень «просит о помощи». Почему поражается печень при сахарном диабете, как распознают и лечат ее болезни – на эти и другие вопросы вы найдете ответ в нашей статье.
Природа наделила печень многообразными ролями. Во-первых, это пищеварительная железа, выделяющая желчь. В перерывах между приемами пищи желчь накапливается в желчном пузыре, откуда во время еды выделяется в кишечник и участвует в переваривании жиров. Во-вторых, именно в печени происходят десятки разнообразных биохимических процессов. Не зря ее называют «центральной биохимической лабораторией». Прежде всего, следует упомянуть о роли печени в обмене углеводов. После еды огромные количества глюкозы устремляются из кишечника в печень с кровью по воротной вене. Печень запасает глюкозу в виде резервного вещества гликогена, тем самым препятствует чрезмерному повышению сахара крови после еды. В перерывах между приемами пищи, печень расщепляет гликоген и не дает уровню сахара крови опуститься слишком низко. А при длительном голодании, когда запасы гликогена иссякают, печень начинает вырабатывать глюкозу из веществ неуглеводной природы.
Роль печени в обмене липидов также весьма существенна. Печень служит главным местом синтеза холестерина, который доставляют каждой клетке организма липопротеины низкой плотности (ЛПНП). Избыток холестерина собирают и переносят обратно в печень липопротеины высокой плотности (ЛПВП). От баланса между этими процессами зависит уровень холестерина в крови и связанный с ним риск атеросклероза. Велика роль печени в обмене белков: в ней образуется большинство белков крови, а токсичные продукты распада белков превращаются в безвредную мочевину. И, наконец, в-третьих, следует сказать о барьерной функции печени: вся кровь, оттекающая от кишечника, проходит через печень. С водой и пищей мы получаем не только полезные питательные, но и чужеродные вещества. Некоторые из них крайне токсичны. В большинстве случаев печень превращает эти вещества в менее опасные и способствует их выведению из организма.
Что же происходит с печенью при сахарном диабете? Главное проявление страдания печени при диабете 1 и 2 типа – это избыточное отложение жира в ней – жировой гепатоз. Достаточно сказать, что здоровая печень содержит 1-2% жира, а при жировом гепатозе его содержание достигает 50%. Избыток жира накапливается в печени вследствие нарушения регуляции обмена веществ инсулином. При диабете 1 типа этот процесс развивается при длительной декомпенсации заболевания. А вот при диабете 2 типа, как правило, жировой гепатоз предшествует развитию диабета – у многих тучных пациентов, привыкших к перееданию, эта проблема обнаруживается еще до повышения сахара крови. На стадии жирового гепатоза болезнь, как правило, ничем себя не проявляет – больной не чувствует недомогания и не спешит к врачу. Лишь при осмотре и УЗИ врач обнаружит увеличенную печень. Следует заметить, что если печень увеличивается медленно и незначительно, то это не вызывает боли. Появление боли в правом подреберье чаще всего связано с патологией желчевыводящих путей, которая также часто встречается при ожирении. Нелеченный жировой гепатоз переходит в более тяжелую стадию: к отложению жира присоединяется воспаление печени – стеатогепатит. Эта стадия находит отражение в биохимическом анализе крови, в частности – повышается активность печеночных ферментов – АЛТ и АСТ. Многолетнее существование стеатогепатита грозит разрастанием в печени соединительной ткани и даже развитием цирроза – грубой деформацией печени с утратой всех ее функций.
Вот почему состояние печени у больного диабетом вызывает тревогу у врачей.
Отражается ли жировой гепатоз на течении сахарного диабета? Оказывается, связь между диабетом и жировым гепатозом обоюдная. Избыточное отложение жира в печени нарушает ее способность регулировать обмен углеводов. Поэтому при жировом гепатозе печень может «пропускать» в кровоток больше глюкозы, чем положено после еды и вырабатывать больше глюкозы натощак. Это часто удивляет пациентов: казалось бы, больной всю ночь ничего не ел, и сахар натощак должен быть низким. Но, вопреки ожиданиям, при наличии жирового гепатоза сахар крови натощак стабильно выше 7 ммоль/л и не снижается при самой жесткой диете.
Какие факторы могут усугубить поражение печени при сахарном диабете? На первое место следует поставить алкоголь. Злоупотребление алкоголем само по себе, при отсутствии ожирения и диабета, способно привести к жировому гепатозу, стеатогепатиту и циррозу. К сожалению, эти два поражающих печень фактора нередко сочетаются у одного больного. Несколько реже встречается сочетание жирового гепатоза при диабете с вирусными гепатитами В и С. Наконец, токсические вещества на производстве, в быту, а также некоторые (к счастью, далеко не все!) лекарства обладают способностью поражать печень. Поэтому при обнаружении проблем с печенью у больного диабетом врач-терапевт или эндокринолог обязательно поинтересуется вашим отношением к алкоголю, полным перечнем применяемых вами лекарств, а также тем, сдавались ли ранее анализы крови на маркеры вирусных гепатитов.
Что же делать для сохранения здоровья печени при сахарном диабете? Прежде всего, контролировать сахар крови и гликированный гемоглобин, советоваться с врачом о правильной сахароснижающей терапии. Важнейшим звеном лечения жирового гепатоза служит правильное питание.
Его принципы такие же, как и при сахарном диабете с ожирением: снижение калорийности рациона за счет легкоусвояемых углеводов и животных жиров. Снижение массы тела при ожирении само по себе оказывает благотворное влияние на печень. Но оно не должно быть слишком быстрым – резкое похудание может усугубить поражение печени. Безопасно медленное снижение веса на 5-10 % от исходного за 6 – 12 месяцев.
Если людям со здоровой печенью можно рассуждать о полезности алкоголя в малых дозах, то при поражении печени алкоголь должен быть совершенно исключен.
Наконец, для восстановления печени применяются разнообразные лекарственные препараты. Остановимся на самых главных из них. Прежде всего, это группа эссенциальных (то есть, незаменимых) фосфолипидов – «строительного материала» для клеток. Прием этих препаратов обеспечивает медленное выведение избытка жира из печени и восстановление поврежденных клеток. Другой широко применяемый препарат – адеметионин. Он особенно показан при злоупотреблении алкоголем. Сегодня, при жировом гепатозе, активно используют препараты урсодезоксихолевой кислоты. Они не только лечат жировой гепатоз, но и снижают риск образования желчных камней. Благотворное действие при жировом гепатозе оказывают и некоторые препараты для лечения сахарного диабета и его осложнений. Способствует снижению выраженности гепатоза широко применяемый метформин, и реже назначаемый пиоглитазон, а также препараты тиоктовой кислоты и таурина.
Разумеется, описание возможностей лекарственный препаратов – это не руководство по самолечению: выбор препарата, дозы и длительность курса определяются врачом исходя из особенностей пациента. Если «печеночные показатели» в биохимическом анализе крови сильно повышены, то лечение часто начинают с внутривенного введения препаратов, а затем продолжают прием таблеток. Как правило, лекарственная терапия длится не менее 3 месяцев, непрерывный прием некоторых препаратов достигает 1 года. Медикаментозную терапию жирового гепатоза в большинстве случаев может назначить врач-терапевт или эндокринолог. Консультация специалиста гастроэнтеролога необходима при неясном диагнозе или обнаружении вирусного гепатита. Поэтому, чтобы узнать о состоянии вашей печени, надо спросить у лечащего врача о результатах биохимического анализа крови, в ряде случаев сделать УЗИ органов брюшной полости.
А вот чего для здоровья печени делать не следует, это проводить так называемые «чистки печени», подробным описанием которых пестрит околомедицинская литература. Смысл таких процедур, как правило, сводится к приему лекарственных растений с желчегонным действием. Если моторика желчевыводящих путей и кишечника ослаблена, это может ее улучшить. Для лечения жирового гепатоза или стеатогепатита это совершенно бесполезно. Ну а при наличии камней в желчном пузыре или протоках может привести больного на операционный стол, если «потревоженный» мелкий камень нарушит отток желчи, вызовет острую боль и желтуху!
Итак, если у вас диабет – поинтересуйтесь у врача состоянием вашей печени, правильно питайтесь и при необходимости пройдите курс лечения. Этим вы поможете печени остаться здоровой на долгие годы!
Источник
Очистка печени при сахарном диабете в домашних условиях
Сахарный диабет — сложнейшее, коварное и смертельно опасное заболевание. Сахарный диабет неизлечим, однако это не приговор. При должном приложении усилий протекание сахарного диабета вполне поддается контролю и благодаря этому, человек, страдающий сахарным диабетом может прожить долгую, счастливую, полноценную жизнь. Сущность сахарного диабета — это глобальное нарушение обмена веществ в организме, приводящее к тому что основной вид энергии (глюкоза или сахар), используемый организмом для продолжения своей жизнедеятельности прекращает или полностью или частично усваиваться организмом, что приводит к тому что его не усвоенный излишек остается в крови и приводит к разрушению кровеносной системы организма, а следовательно в дальнейшем к разрушению всех остальных систем организма.
Особенностью сахарного диабета является то, что медикаментозное лечение, несмотря на то , что без него в подавляющем количестве случаев не обойтись (просто из за запущенности болезни), является вспомогательным средством.
Основой же лечения сахарного диабета является очистка организма от шлаков, и излишков других веществ, вызванных нарушением обмена веществ. При этом необходимо учитывать, что на человека, страдающего сахарным диабетом накладываются ограничения вызванные изменениями, произошедшими в его организме за время развития его болезни, а это делает большую часть стандартных методов (типа употребления растительного масла или голодания) не просто бесполезными, но и потенциально опасными.
Главным и единственным средством очищения организма (в т.ч. и печени), а значит лечения и контроля сахарного диабета является сбалансированная диета. Сущность правильного питания при сахарном диабете заключается в следующем:
Сокращение употребления богатой насыщенными жирами пищи (жирные сорта мяса или молочные продукты с большим содержанием жира). Отдельной строкой стоит выделить печень животных или птиц. Употребление печени очень полезно, т. к. они содержат массу витаминов и веществ, способствующих нормализации уровня холестерина. При этом нужно не забывать, что печень, в отличии от мяса, содержит в себе углеводы, по этому употреблять только в варенном или тушеном виде, небольшими порциями исключительно с овощами. Так же следует остановиться на куриной и говяжьей печени, т. к. остальные содержат большое количество жира.
Увеличение в рационе доли овощей и фруктов
Исключение из рациона сахаросодержащих продуктов (пирожные, сладкая выпечка)
Снижение употребления соли во всех видах (соленые продукты, копчености)
Стараться избегать блюд, приготовленных с помощью ингредиентов содержащих большое количество жиров, таких как масла, майонез, сметана и т. д.
Таким образом в результате ограничений, которые диктует сахарный диабет особе значение для очистки печении приобретают сборы, фиточаи и моносоставы лекарственных трав:
«Лапчатка Белая»
Лапчатка белая — многолетнее лекарственное растение, известное с восемнадцатого века. В народной медицине применяется для нормализации общего обмена веществ в организме, особенно эффективна для восстановления функций щитовидной железы. Обладает антигипертензивным действием, благотворно влияет на стенки сосудов, что снижает последствия разрушительного воздействия повышенного содержания глюкозы в крови. Нормализует работу печени, способствует снижению содержания холестерина. Хорошо подходит для длительного применения.
Дополнительный плюс лапчатки белой практически полной отсутствие противопоказаний, за исключением повышенной индивидуальной чувствительности, перед употреблением во время беременности необходимо проконсультироваться с врачом.
«Шиповник»
Полезные свойства шиповника известны человечеству еще с конца последнего ледникового периода, он обладает могучим антибактериальным действием, великолепно зарекомендовал себя как профилактической средство для поддерживания иммунитета, что при сахарном диабете имеет одно из важнейших значений, особенно у детей. Так же шиповник является хорошим желчегонным средством, нормализует давление, способствует нормализации уровня холестерина.
Исключительно при индивидуальной чувствительности.
Источник
Неалкогольная жировая болезнь печени у пациентов с сахарным диабетом 2 типа: особенности патогенеза и лечения
Л. А. Звенигородская 1 , A.M. Мкртумян 1,2 , Т.В. Нилова 1 , М.В, Шинкин 1 , А.В. Петраков 1
1 ГБУ «Московский клинический научно-практический центр» Департамента здравоохранения Москвы
2 ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова»
Опубликовано в журнале: «Эффективная фармакотерапия» 2017г.
Неалкогольная жировая болезнь печени (НАЖБП) в настоящее время является одним из самых распространенных заболеваний в гепатологии. Важным патогенетическим аспектом развития НАЖБП считается дисбаланс желчных кислот.
У больных сахарным диабетом (СД) заболевание встречается в 85-90% случаев. При СД2 типа и инсулинорезистентности эндокринная функция желчных кислот нарушается, уменьшается их абсорбция. Как следствие, увеличивается жировая инфильтрация печени, нарушается метаболизм липидов, происходит накопление триглицеридов и липопротеинов низкой плотности в печени и плазме. Уменьшение циркулирующих желчных кислот приводит к развитию билиарной недостаточности и прогрессированию НАЖБП. В патогенезе НАЖБП немаловажную роль также играет дефицит таурина. Он участвует во всех видах обмена веществ. Кроме того, таурин снижает содержание продуктов жизнедеятельности микроорганизмов в толстой кишке (короткоцепочечных жирных кислот, эндотоксина, оксида азота). Таурин (Дибикор) оказывает противовоспалительное, антиоксидантное, детоксицирующее и мембраностабилизирующее действие. Его прием ассоциируется с уменьшением степени активности неалкогольного стеатогепатита у пациентов c НАЖБП и СД2 типа.
Ключевые слова: неалкогольная жировая болезнь печени, желчные кислоты, оксид азота, эндотоксин, таурин, комплексное медикаментозное лечение
Введение
Неалкогольная жировая болезнь печени (НАЖБП) уже несколько десятилетий является предметом пристального внимания врачей разных специальностей. НАЖБП признана основным компонентом метаболического синдрома и главным фактором риска развития сердечнососудистых осложнений 2. Поражение печени при данном заболевании характеризуется жировой дистрофией (стеатоз) с воспалением и повреждением гепатоцитов (неалкогольный стеатогепатит (НАСГ)) и развитием фиброза. При прогрессировании существует риск перехода НАЖБП в цирроз. В 75% случаев НАЖБП сочетается с ожирением, дислипидемией, артериальной гипертензией, сахарным диабетом (СД) 2 типа или нарушением толерантности к глюкозе (НТГ) [1, 5, 6]. Указанные патологические процессы относятся к факторам риска прогрессирования атеросклероза и развития сердечно-сосудистых заболеваний. Определенная роль в патогенезе НАЖБП отводится снижению синтеза и нарушению транспорта желчных кислот (ЖК), что обусловлено повреждением мембран гепатоцитов, ингибированием ферментных систем и воспалением.
Желчные кислоты — стероидные монокарбоновые кислоты, производные холановой кислоты. Они образуются в гладком эндоплазматическом ретикулуме гепатоцитов и являются секретом эпителиальных клеток печени. Биосинтез ЖК считается одним из важных путей выведения холестерина (ХС). Пул ЖК у человека представлен примерно в равных количествах высокогидрофобными холевой, хенодезоксихолевой, дезоксихолевой кислотами. Первичные ЖК конъюгируются с глицином и таурином, что повышает их гидрофильность. Они являются активаторами ядерных рецепторов, регулирующих экспрессию генов, участвующих в секреции, транспорте и метаболизме первичных ЖК, ХС и триглицеридов (ТГ) в гепатоцитах и плазме [3, 7, 8]. При СД 2 типа и инсулинорезистентности (ИР) эндокринная функция ЖК нарушается, уменьшается их абсорбция, что увеличивает жировую инфильтрацию печени, нарушает метаболизм ли-пидов, в печени и плазме накапливаются ТГ и липопротеины низкой плотности (ЛПНП). Развивается билиарная недостаточность, приводящая к уменьшению количества желчи и циркулирующих Ж К. Как следствие, развиваются жировая болезнь печени и холелитиаз [3, 4, 6, 9-12].
ЖК являются активаторами липолитических ферментов, повышают активность липазы в 10-15 раз. В крови желчные кислоты транспортируются главным образом с альбумином, а также с липопротеинами высокой плотности (ЛПВП).
Образование желчи, транспорт ЖК связан с активностью Na/K-АТФазы, играющей важную роль в захвате гепатоцитами хлоридов и бикарбонатов из плазмы. Нарушение активности Na/K-АТФазы обусловливает снижение чувствительности рецепторов к инсулину.
Нарушение транспортных функций гепатоцитов приводит к на-рушению метаболизма лекарств, изменению их токсичности и эффективности.
При воспалении значительно снижается активность многих белков-транспортеров. В первую очередь происходят нарушения в мембранных белках транспортеров глюкозы. Это приводит к ИР, провоцирует развитие сосудистой воспалительной реакции из-за избыточной продукции жировой тканью воспалительных цитокинов [4, 10, 12]. Перекисное окисление липидов подавляет активность ферментов — цитохромоксидазы (таким образом угнетается тканевое дыхание) и гидроксилазы (участвует в превращении холестерола в ЖК). Под влиянием активных форм кислорода нередко образуются аномальные формы ЖК, липопротеинов, липидов и других продуктов секреции желчи. Как следствие, изменяются их физико-химические свойства, физиологические функции и развивается и прогрессирует НАСГ. Пероксинитрит тормозит ферменты дыхательной цепи митохондрий — мембранную Na/K-АТФазу и блокирует натриевые каналы. Избыток в клетках свободных жирных кислот (СЖК) усиливает продукцию активных форм кислорода, активизируется синтез эндотелием синтазы оксида азота (NO) и его образование. При избытке СЖК уменьшается связывание инсулина рецепторами гепатоцитов и развивается гиперинсулинемия. Инсулин стимулирует образование NO. Высокая продукция N0 наблюдается при эндотоксинемии, септическом шоке и увеличенной кишечной проницаемости при воспалительных заболеваниях кишечника [13, 14].
Эндотоксинемия угнетает антиоксидантную систему, что сопровождается повышением деконъюгации ЖК, образованием токсичных солей и повышением реабсорбции. При этом синтез ЖК уменьшается, ХС — увеличивается. В патогенезе НАЖБП немаловажную роль играет дефицит таурина. Таурин — жизненно необходимая сульфоаминокислота, которая является конечным продуктом обмена серосодержащих аминокислот (метионина, цистеина, цистеамина) [15, 16]. Молекула таурина состоит из двух атомов углерода, сульфоновой группы (S03H) и аминогруппы (NH ). Однако биологически синтезируемого таурина недостаточно для поддержания биохимических процессов в организме, в которых он задействован. Основным источником таурина считаются мясные и рыбные продукты. При недостаточности поступления таурина с пищей или вследствие каких-либо иных причин (ишемия, СД, стресс, травма и др.) страдают все виды обмена веществ в каждой клетке каждого органа. Так, дефицит таурина в печени ассоциируется с нарушением выделения желчи, образованием камней, изменением обмена ХС и липидов.
Известно, что таурин, соединяясь с холевой кислотой, участвует во всасывании жиров и жирорастворимых витаминов. Таурин может соединяться с атомом хлора, источником которого является гипохлорная кислота, производимая активированными нейтрофилами. В данном случае таурин выступает в качестве окислителя и компонента антибактериальной защиты. В митохондриях хлораминотаурин влияет на сборку белков дыхательной цепи и оказывает антиоксидантное воздействие. Это соединение уменьшает воспалительный сигнал в клетках животных через ингибирование активации нуклеарного фактора каппа В. В свободном состоянии таурин выполняет жизненно важную для животной клетки функции — регуляцию осмотического давления и ионов кальция.
При недостаточном поступлении таурина с пищей или вследствие каких-либо иных причин (ишемия, СД, стресс, травма и др.) страдают все виды обмена веществ в каждой клетке каждого органа. Так, дефицит таурина в печени ассоциируется с нарушением выделения желчи, образованием камней, изменением обмена ХС и липидов
Таурин участвует в регуляции желчевыделения. Первичные ЖК (холевая и хенодезоксихолевая) синтезируются в гепатоцитах печени из ХС. Вторичные (литохолевая, урсодезоксихолевая, аллохолевая и др.) — образуются из первичных в толстой кишке.
В желчном пузыре ЖК присутствуют главным образом в виде конъюгатов — парных соединений с глицином и таурином. Продуктом конъюгации ЖК с таурином являются таурохолевая, таурохенодезоксихолевая и тауродезок-сихолевая кислоты. Конъюгация с ЖК обеспечивает их устойчивость — не выпадают в осадок при низких значениях рН в желчных протоках и двенадцатиперстной кишке. Важная роль ЖК в пищеварении заключается в способствовании всасыванию ряда гидрофобных веществ: ХС, жиров, жирорастворимых витаминов, растительных стероидов. В отсутствие ЖК всасывание вышеперечисленных компонентов пищи практически невозможно. Таурохолевая кислота снижает количество Escherichia coli в слепой кишке [17].
В отличие от ЖК, конъюгированных с глицином, тауроконъюгаты ЖК обладают холеретическим действием и предупреждают развитие холестаза [18, 19]. В исследовании in vitro гликолитохолевая кислота легко осаждается кальцием, чего не наблюдается с тауролитохолевой кислотой [13]. Таким образом, таурин необходим для повышения текучести желчи, увеличения продукции ЖК и предупреждения развития холестаза [14, 20].
Таурин снижает содержание продуктов жизнедеятельности микроорганизмов в толстой кишке (короткоцепочечных жирных кислот, эндотоксина, оксида азота) 23.
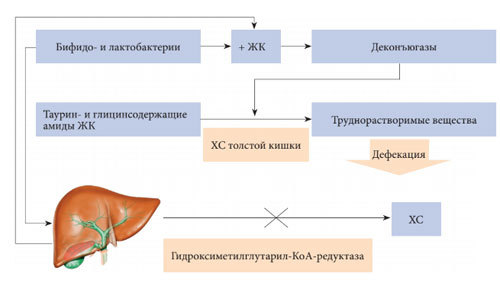
При диффузных заболеваниях печени таурин увеличивает кровоток, улучшает микроциркуляцию и уменьшает выраженность цитолиза [24]. Доказано его положительное влияние на углеводный и липидный обмен. Антиоксидантное, гипогликемическое, детоксицирующее действие таурина и его способность выводить ХС (рис. 1) позволяют рассматривать его в качестве препарата для терапии НАЖБП. У больных СД таурин уменьшает ИР, защищает бета-клетки поджелудочной железы, оказывает сахароснижающее действие, не вызывая развития гипогликемии [14,20].
Рис. 1. Схема выведения ХС
В деконъюгации комплексов ЖК с таурином и глицином активно участвуют ферменты различных бактерий. В норме дезоксихолевая и хенодезоксихолевая кислоты при участии секреторного иммуноглобулина А, влияющего на их антимикробную активность, подавляют рост патогенных и условно патогенных микроорганизмов даже в физиологических концентрациях [2]. При нарушении энтерогепатической циркуляции ЖК образуется их значительный дефицит в кишечнике. В тонкой кишке недостаток ЖК обусловливает изменение работы всего пищеварительно-транспортного конвейера, нарушение всасывания и переваривания пищи (синдром нарушенного всасывания). В толстой кишке их дефицит (помимо многочисленных метаболических нарушений) ассоциируется со снижением «стерилизующих» и нутритивных свойств желчи. Прогрессирование дисбиоза, брожение, дисфункция баугиниевой заслонки и усиление микробной контаминации тонкой (подвздошной) кишки, с одной стороны, поддержание хронического воспаления в печени вследствие поступления через систему воротной вены с кровью повышенного количества эндотоксина грамотрица-тельной микрофлоры — с другой, способствуют прогрессированию стеатогепатита (рис. 2 и 3). В связи с вышеизложенным необходимым условием эффективного лечения НАЖБП представляется восстановление энтерогепатической циркуляции желчных кислот: нормализация синтеза желчи в печени и ее адекватное поступление в кишечник [25]. Поэтому назначение препаратов, одновременно обеспечивающих антиоксидантную защиту, стабилизацию мембран гепатоцитов, противо-воспалительное действие, нормализацию состава метаболитов кишечной микрофлоры, обоснованно.
В ходе исследования было поставлено три цели:
1) определить общее содержание ЖК в сыворотке крови пациентов с НАЖБП и СД 2 типа;
2)оценить влияние маркеров воспаления (NO, эндотоксина, фосфолипазы А2 (ФЛА2), малонового диальдегида (МДА)) на синтез и транспорт ЖК;
3) проанализировать фармакодинамические показатели метаболитов NO и бактериального эндотоксина, биохимические показатели крови и липидного спектра на фоне трех месяцев терапии таурином (препаратом Дибикор) у больных НАЖБП и СД 2 типа.
Материал и методы исследования
Обследовано 158 пациентов с НАЖБП (90 женщин и 68 мужчин). Средний возраст больных -55,5 ± 7,5 года. С СД 2 типа 46 пациентов, с НТГ — 112. Индекс массы тела более 30 кг/м 2 . Диагноз верифицирован клиническими, биохимическими, инструментальными и морфологическими методами. Общее содержание ЖК в сыворотке крови определяли ферментным методом на биохимическом анализаторе Olimpus с использованием тест-систем Randox (Англия). Содержание ФЛА2 определяли иммуноферментным методом с использованием диагностических наборов PLAC TEST ELiSA Kit (США). Перекисное окисление липидов определяли по содержанию МДА с тиобарбитуровой кислотой. Для определения эндотоксина применяли хромогенный метод по конечной точке с использованием LAL-теста (Limulus Amebo-cyte Lysate). Уровень метаболитов NO оценивали скрининг-методом в биологических жидкостях с хлоридом ванадия (Германия). В двойное слепое плацебоконтролируемое исследование включено 40 больных, страдающих НАЖБП и СД 2 типа: 30 женщин и 10 мужчин. Их средний возраст составил 56,35 ± 8,75 года. Методом случайных чисел пациентов разделили на две группы. Первая (основная группа) получала таурин (Дибикор, ООО «ПИК-ФАРМА»), вторая (контрольная группа) -плацебо.
Дибикор назначали в дозе 0,5 г два раза в день за 20 минут до еды. Длительность применения — три месяца. Статистическую обработку данных проводили с использованием программы «Биостат»
Результаты и их обсуждение
Общее содержание ЖК в сыворотке крови. У больных НАЖБП без нарушения углеводного обмена (68 пациентов) среднее содержание ЖК в сыворотке крови составило 5,4 ± 1,8 мкмоль/л. У больных НАЖБП с НТГ — 8,88 ± 4,94 мкмоль/л. У 59 пациентов с НАЖБП и СД 2 типа их содержание было достоверно снижено на 45% и составило 2,97 ± 0,2 мкмоль/л (р = 0,001). У пациентов с НАЖБП, которая наблюдается при ожирении в 90% случаев [1, 3], изменяется состав желчи, увеличивается ее литогенность и развиваются билиарный сладж и холелитиаз. Желчные кислоты регулируют метаболизм глюкозы и липидов. Биосинтез и транспорт ЖК связан с активностью фермента Na/K-АТФазы. ЖК восстанавли-вают чувствительность рецепторов к инсулину [4, 6, 9, 12], лептину, грелину и адипонектину
При развитии воспаления снижается активность НОТ4-альфа (гепатоцитарный ядерный фактор для синтеза и конъюгации ЖК) [4, 6, 9, 10, 12].
Оксид азота ингибирует и блокирует натриевые каналы, подавляет активность фермента холестерол-гидроксилазы, осуществляющей превращение холестерола в ЖК. При воспалении,гипоксии, эндотоксиновой агрессии нарушаются функции эндотелия. Макрофаги под действием эндотоксина выделяют NO, который легко проникает в клетки и взаимодействует с ферментами и белками-переносчиками, влияет на конъюгацию ЖК, липопротеинов и глюкозы. Уровень стабильных метаболи-тов NO в группе НАЖБП и СД 2 типа оказался достоверно выше и составил в среднем 137,7 ± 35,96 мкмоль/л по сравнению с группой НАЖБП и НТГ и контрольной группой — 66,75 ± 17,01 и 32,15 ± 0,51 мкмоль/л (р = 0,0001). Содержание метаболитов NO возрастало параллельно концентрации аминотрансфераз (r = 0,86) и ФЛА2 (r= 0,658). ФЛА2 гидролизует окисленный фосфатидилхолин с образованием жирной кислоты и лизофосфатидилхолина, который изменяет активность синтазы NO и количество синтезируемого NO или снижает его биодоступность.
Утилизация глюкозы в жировой и мышечной тканях NO-зависима, при блокировании как нейрональной, так и эндотелиальной NO-синтазы развивается гипергликемия [19]. Оксид азота ингибирует Na/K-АТФазу. В результате снижается чувствительность к инсулину, ингибируются митохондриальные ферменты, цитохром Р-450, который метаболизирует ЖК и ХС, происходит накопление СЖК в клетках печени. Уровень ФЛА2 в сыворотке крови пациентов с НАЖБП и СД 2 типа в среднем составил 621,9 ± 84,71 нг/мл (медиана — 605 (504-826) нг/мл) (р = 0,0001), пациентов с НАЖБП и НТГ — 423,2 ± 45,2 нг/мл (медиана — 430 (324-497) нг/мл) (р = 0,0001).
При попадании в кровоток ФЛА2 связывается и транспортируется с ЛПНП. Между ФЛА2 и ЛПНП отмечена корреляционная зависимость (r = 0,957): чем выше в плазме крови уровень ХС ЛПНП, тем более активно формируется атероматоз интимы артерий, тем в большей степени выражен дефицит в клетках эссенциальных полиеновых жирных кислот. Как следствие, повышается вязкость фосфолипидов в мембране клеток, нарушается функция белков мембраны, в том числе глюкозных транспортеров, что приводит к развитию к СД 2 типа. Содержание эндотоксина в сыворотке крови в группе НАЖБП и СД 2 типа было увеличено в 12 раз по сравнению с содержанием эндотоксина в контрольной группе — 3,69 ± 1,44 ЕЭ/мл (норма — 0,3 ± 0,05 ЕЭ/мл). В группе НАЖБП и НТГ его уровень составил 1,43 ± 0,24 ЕЭ/мл (р = 0,0001). Повышение эндотоксина и NO выявлено при прогрессировании воспалительной инфильтрации в печени (рис. 4). Эндотоксин активирует Са 2+ -каналы на мембране гладкомышечных клеток, что приводит к активации ФЛА2. Показатели перекисного окисле-ния липидов. Содержание МДА у пациентов с НАЖБП и СД 2 типа в зависимости от степени выраженности воспаления оказалось увеличенным в два раза. При гипергликемии и чрезмерном накоплении липидов в гепатоцитах усиливаются процессы перекисного окисления первых, что проводит к некрозу гепатоцитов, нарушению функции митохондрий, развитию фиброза и формированию стеатогепатита (см. рис. 2-4).
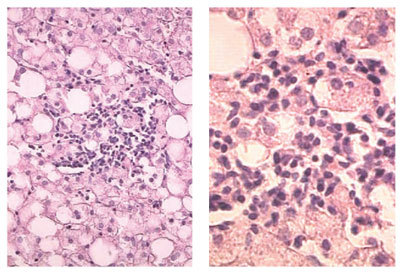
Рис. 2. Смешанноклеточный внутридольковый инфильтрат при стеатогепатите (500-кратное увеличение)
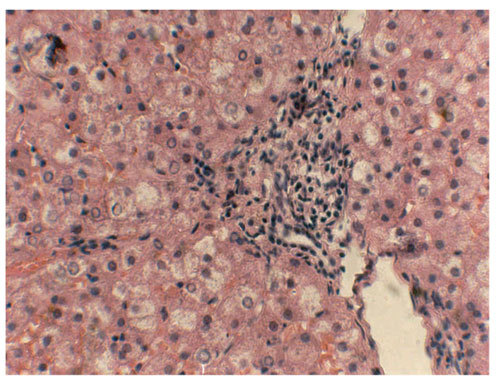
Рис. 3. Небулярный гепатит у пациентов с СД 2 типа и НАЖБП (400-кратное увеличение)
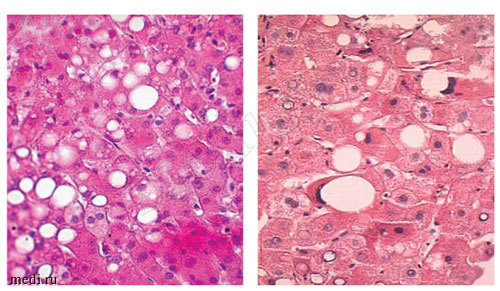
Рис. 4. Жировая инфильтрация гепатоцитов при стеатозе печени (500-кратное увеличение)
Выявлена также связь перекисного и фосфолипазного механизмов повреждения мембран гепатоцитов. Отмечена корреляционная зависимость между ФЛА2 и МДА. Коэффициент корреляции —578 (р = 0,005).
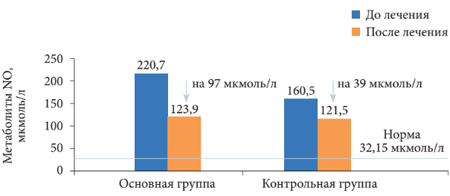
Уровень метаболитов NO у па-циентов с НАЖБП и СД 2 типа до лечения был повышен в 6,8 раза и составлял 220,7 ± 14,27 мкмоль/л (норма — 32,15 ± 0,51 мкмоль/л) (р = 0,001). После лечения Дибикором их содержание снизилось на 97 мкмоль/л (на 44%) (рис. 5). Лечение таурином сопровождалось улучшением биохимических показателей крови. Отмечалось снижение общего ХС (ОХС), ХС ЛПНП и ТГ, нормализация липидного спектра. Уровень метаболитов NO уменьшался одно-временно с уменьшением уровня аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT) и гамма-глутамилтранспептидазы (ГГТП) (таблица, рис. 6 и 7). Таким образом, у пациентов с НАЖБП и СД 2 типа отмечено снижение уровня ЖК на 45%, что связано с повреждением мембран клеток, ингибированием ферментных систем и воспалением. Увеличение содержания маркеров воспаления липопротеин-ассоциированной ФЛА2, NO, эндотоксина, МДА при НАЖБП и СД 2 типа связано с воспалительным процессом в печени с повышением активности печеночных ферментов и тяжелыми морфологическими изменениями.
Рис. 5. Содержание метаболитов NO у пациентов с НАЖБП и СД 2 типа до и после лечения
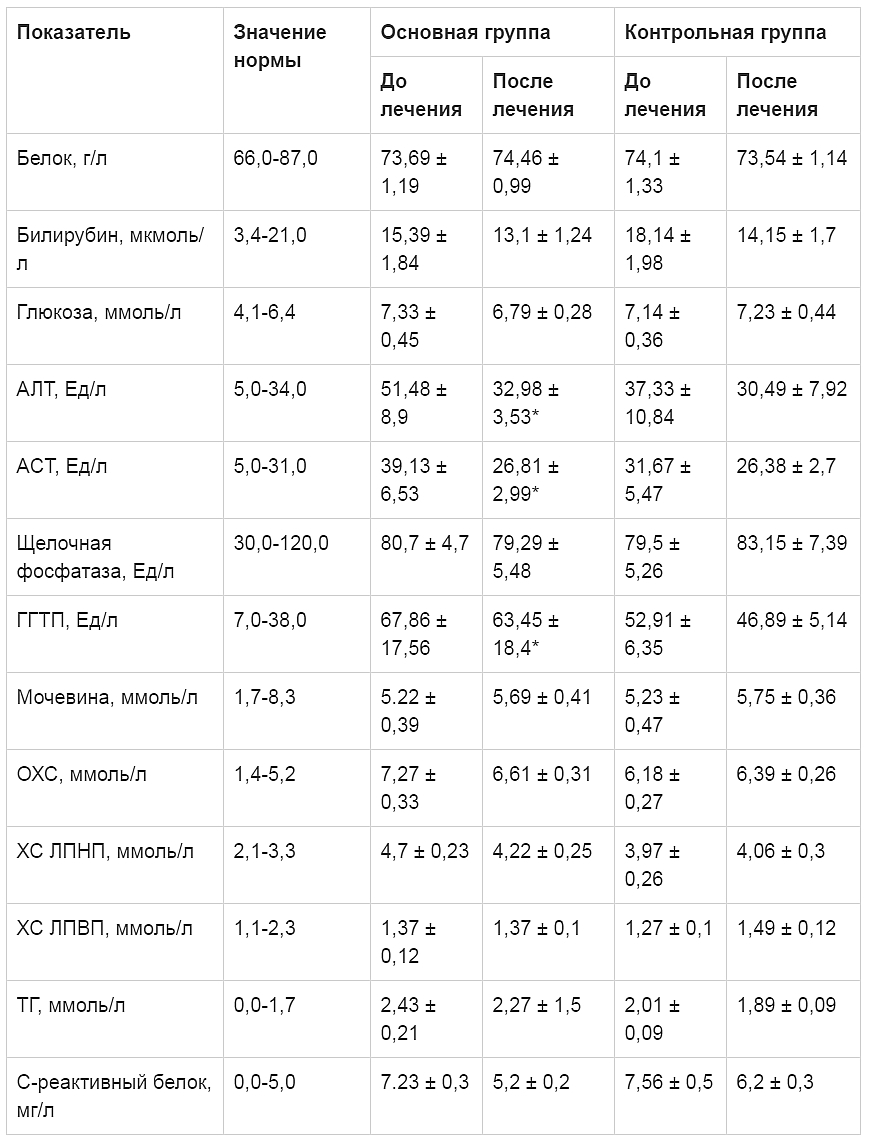
Таблица. Динамика биохимических показателей крови у пациентов с НАЖБП и СД 2 типа до и после лечения
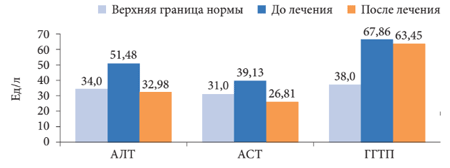
Рис. 6. Динамика биохимических показателей крови на фоне лечения Дибикором
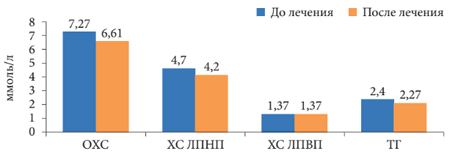
* р Рис. 7. Динамика липидного спектра крови на фоне терапии Дибикором
Заключение
Полученные результаты свидетельствуют о противовоспалительном, антиоксидантном, детоксицирующем и мембраностабилизирующем действии Дибикора у пациентов с НАЖБП и СД 2 типа. На фоне приема препарата уменьшалась активность НАСГ, что сопровождалось улучшением биохимических показателей крови и липидного спектра (отмечена тенденция к снижению ОХС, ХС ЛПНП, увеличению ХС ЛПВП), снижением уровня метаболитов NO параллельно снижению уровня АЛТ, ACT и ГГТП.
Литература
1. Лазебник Л.Б., Звенигородская Л.А. Метаболический синдром и органы пищеварения. М., 2009.
2. Tazume S., Yamaoka Т., Hashimoto К., Sasaki S. Intestinal flora and bile acide metabolism. Quantitative analysis of bile acide metabolites in each step of rejection of Shigella organisms // J. Germfree Life Gnotobiol. 1978. Vol. 8. № 2. P. 61-67.
3. Ивашкин В.Т., Маевская М.В. Липотоксичность и метаболические нарушения при ожирении // Российскийжурнал гастроэнтерологии, гепатологии, колопроктологии. 2010. № 1. С. 4-13.
4. Roy D., Perreault М., Marette A. Insulin stimulation of glucose uptake in skeletal muscles and adipose tissues in vivo is NO dependent // Am. J. Physiol. 1998. Vol. 274. № 4. Pt. 1. P. E692-699.
5. Урсова Н.И. Жировая дистрофия печени при метаболическом синдроме в практике врача-педиатра // Лечащий врач. 2010. № 1. С. 14-17.
6. Ивашкин В.Т. Ядерные рецепторы и патология печени (часть 2) // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2010. № 4. С. 7-15.
7. St-Pierre М.V., Kullak-Ublick G.A., Hagenbuch В., Meier P.J. Transport of bile acids in hepatic and non-hepatic tissues // J. Exp. Biol. 2001. Vol. 204. Pt. 10. P. 1673-1686.
8. Максимов B.A.,Чернышев А.Л., Тарасов K.M., Неронов В.А. Билиарная недостаточность. Этиология, патогенез, клиника, диагностика, лечение. М., 2008.
9. Ивашкин В. Т. Ядерные рецепторы и патология печени (часть 1) // Российский журнал гастроэнтерологии, ге-патологии, колопроктологии. 2010. № 3. С. 4-8.
10. Lefebvre P., Cariou В., Lien F. et al. Role of bile acids and bile acid receptors in metabolic regulation // Physiol. Rev. 2009. Vol. 89. № 1. P. 147-191.
11. Подымова С.Д. Современные представления о патогенезе и терапии внутрипеченочного холеста-за // Русский медицинский журнал. 2001. Приложение «Болезни органов пищеварения». № 2. С. 66 // www.rmj.ru/articles/bolezni_organov_pishchevareniya/ Sovremennye_predstavleniya_o_patogeneze_i_terapii_ vnutripechenochnogo_holestaza/.
12. Шептулина А.Ф., Широкова Е.Н., Ивашкин В.Т. Ядер-ные рецепторы в регуляции транспорта и метаболизма желчных кислот // Российский журнал гастроэнтероло-гии, гепатологии, колопроктологии. 2013. № 5. С. 32-45.
13. Yamori Y, Taguchi Т., Hamada A. et al. Taurine in health and diseases: consistent evidence from experimental and epidemiological studies // J. Biomed. Sci. 2010. Vol. 17. Suppl. 1. P. S6.
14. Ворохобина H.B., Кузнецова A.B. Применение Дибико-ра* у больных с сахарным диабетом 2 типа и метабо-лическим синдромом // Русский медицинский журнал. 2010. № 23. С. 1429-1433.
15. Недосугова Л.В. Место Дибикора в комплексной те-рапии сахарного диабета // Фарматека. 2008. № 17. С. 22-27.
16. Han /., Bae J.H., Kim S.Y. et al. Taurine increases glucose sensitivity of UCP2-overexpressing beta-cells by ameliorat-ing mitochondrial metabolism // Am. J. Physiol. Endocr. Metab. 2004. Vol. 287. № 5. P. 1008-1018.
17. Калинина E.B., Черное H.H., Алеид P. и др. Современные представления об антиоксидантной роли глутатиона и глутатионзависимых ферментов // Вестник РАМН. 2010. № 3. С. 46-54.
18. Стеновая Е.А., Петина Г.В., Жаворонок Т.В и др. Роль тиолдисульфидной системы в механизмах изменений функциональных свойств нейтрофилов при окислительном стрессе // Бюллетень экспериментальной биологии и медицины. 2010. Т. 150. № 8. С. 161-165.
19. Метельская В.А., Туманова Н.Г. Скрининг-метод определения уровня метаболитов оксида азота в сыворотке крови // Клиническая лабораторная диагностика. 2005. № 6. С. 15-18.
20. Елизарова Е.П. Применение Дибикора в кардиологической практике. Пособие для врачей. М., 2005.
21. Титов В.Н, Дугин С.Ф. Синдром транслокации, липополисахариды бактерий, нарушения биологических реакций воспаления и артериального давления (лекция) // Клиническая лабораторная диагностика. 2010. № 4. С. 21-37.
22. Шварц В. Воспаление как фактор патогенеза ИР и СД 2 типа // Терапевтический архив. 2009. № 10. С. 74-80.
23. Покровский В.И., Виноградов Н.А. Оксид азота, его физиологические и патофизиологические свойства // Терапевтический архив. 2005. № 1. С. 82-87.
24. Ogata Y, Nishi М., Nakayama Н. et al. Role of bile in intestinal barrier function and its inhibitory effect on bacterial translocation in obstructive jaundice in rats // J. Surg. Res. 2003. Vol. 115. № 1. P. 18-23.
Источник